Хлорид натрия при травме
Для начала хочется отметить, что это обзорная статья, цель которой не углубиться в патофизиологию, патогенез шока, развитие коагулопатии, метаболического ацидоза и других состояний, сопровождающих шок, вызванный кровотечением. Об этом мы будем рассказывать последовательно и отдельно, но вышеупомянутых аспектов все равно немного коснемся. Сегодня рассмотрим применение «Физиологического раствора» или «Normal Saline».
Немного базовой химии: кристаллоид – вещество, легкорастворимое и способное проходить в растворённом виде через мембраны, проницаемые для жидкости, то есть вещество, способное образовывать истинные растворы. Классический пример кристаллоида — раствор поваренной соли в воде. Таким образом, физраствор, который представляет из себя р-р 0.9% NaCl, относится к кристаллоидам.
Физраствор (точнее, его аналоги) существует уже почти 200 лет, восходя своими корнями к пандемии холеры в Европе в 1831г. Считается, что первый зарегистрированный эксперимент по современной внутривенной инфузионной терапии был проведен русским химиком, который при лечении больного холерой «ввел 6 унций (180 мл) физраствора внутривенно».
Уильям Брук О’Шонесси опубликовал статью в журнале Lancet в декабре 1831 года, в которой говорилось, что цель внутривенного введения жидкости при лечении холеры заключалась в следующем: «Восстановить кровь до ее естественного удельного веса; во-вторых, для восстановления дефицита солей, что может быть достигнуто только путем введения водных растворов в вену». Конечно, тогда «физраствор» не был физиологическим (и сейчас не является), но он не представлял из себя чистый раствор поваренной соли. Позже было проведено множество экспериментов с составом, что породило ряд иных кристаллоидов – дисоль, трисоль и иные.
В 1830-х годах многие практикующие врачи экспериментировали с различными составами, пытаясь «восстановить естественный кровоток в венах и артериях» и «улучшить цвет крови».
В мае 1832 года Роберт Левинс описал метод , который Томас Латта использовал на шести пациентах, терапия велась с помощью растворов, состоящих из «двух драхм соляной кислоты и двух скрупулей карбоната соды на 60 унций воды». Также присутствовали и другие пропорции.
По мере того, как в 1833 году пандемия холеры пошла на спад, потребность в исследованиях жидкостей для внутривенного введения отпала, и в течение последующих лет исследования и публикации были достаточно редки.
Впервые термин «нормальный физиологический раствор» появляется в выпуске «Ланцета» в сентябре 1888 года. Согласно статье «пациенту, который более месяца страдал от рвоты при минимальном приеме пищи, было введено 34 унции раствора (1020 мл) Чертона». «Раствор Чертона» – еще один экспериментальный состав, также далекий от «нормального физраствора» и от любого другого современного кристаллоида, включавший в себя карбонаты и фосфаты.
Когда появился современный состав, и концентрация в 0.9%, не ясно.
Только в 1921м году датский химик Хартог Якоб Хамбургер доказал, что «плазма крови изотонична 0.9% раствору хлорида натрия», это сочли подтверждением целесообразности использования физраствора в клинической практике в качестве кровезамещающего препарата. При этом конкретно 0.9% р-р NaCl не назывался ни «нормальным», ни «физиологичным».
На данный момент препарат используется при кровопотере у пациентов и пострадавших по всему миру, и отказа от него не происходит по разным причинам. Почему физраствор не подходит в качестве препарата выбора при кровопотере?
Физраствор не является кровью
При кровотечении пострадавший теряет кровь, и было бы заблуждением думать, что водой и двумя ионами можно полноценно заменить кровь.
Физраствор, а также аналогичные препараты, такие как Лактат Рингера (LR), являются кристаллоидами и, следовательно, состоят из электролита (в данном случае поваренной соли) и растворителя (вода).
Плазма крови – также является раствором электролитов, но ионный состав плазмы крови далек от «физиологического» раствора. (См. Таблицу ниже).
| Среда | Na+ (ммоль/л) | Cl– (ммоль/л) | K+ (ммоль/л) | Ca2+ (мг/децилитр) | Mg2+ (мг/децилитр) |
| Плазма | 134-145 | 98-107 | 3.6-5.2 | 8.9-10.1 | 1.7-2.3 |
| Физ. р-р | 154 | 154 | 0 | 0 | 0 |
В таблице приведены данные о примерном ионном составе плазмы крови в сравнении с физраствором
Как мы видим, физраствор не соответствует плазме даже по ионному составу, не говоря уже о наличии белков и форменных элементов крови.
Целью инфузионной терапии при кровопотере является восстановление функциональности крови. Мы стремимся вернуть циркулирующий объем, нормализовать доставку кислорода и гемостатический потенциал (функция свертывания). Физраствор не даст нам достичь ни одной из этих целей.
Ранее утверждалось, что физраствор может увеличивать объем циркулирующей крови (ОЦК) и поможет «циркуляции» оставшихся в кровеносном русле эритроцитов для доставки кислорода. Однако, сами кристаллоиды не выполняет эту функцию, важно понимать, что кислород в организме переносит только кровь.
Примечание: вопрос использования кровезаменителей-переносчиков кислорода (КЗПК), таких как растворы модифицированного гемоглобина (МГ) или растворы перфторуглеводородов (ПФУ), например, Перфторан, пока оставим за рамками обсуждения.
Итак, мы вводим растворы не для того, чтобы «просто поддержать давление пострадавшего на определенном уровне», необходимо понимать, что и для чего мы делаем. Простое добавление жидкости в сосудистое русло с целью «подтолкнуть» оставшиеся эритроциты для доставки кислорода и удаления метаболитов не получило документальных научных подтверждений эффективности. Как и утверждения о том, что применение больших объемов кристаллоидов улучшит перфузию (кровоснабжение) органов.
Из-за афизиологичности физраствора (и других несбалансированных кристаллоидов) подобное применение может привести к серьезным осложнениям, включая компартмент-синдром, нарушения свертываемости (коагулопатию), нарушения электролитного баланса (геперхлоремия), снижение рН (ацидоз – создание кислой среды), все эти явления будут системно ухудшать состояние пострадавшего с кровопотерей, дополнительно провоцируя повреждение почек и иммунную дисфункцию (что критично на фоне боевой травмы, которая всегда загрязнена).
При объемной кровопотере, когда пострадавший в состоянии шока (состоянию пониженного кровоснабжения органов с вытекающим недостаточным кислородным и субстратным обеспечением, ведущим к клеточной дисфункции и смерти), его ткани не получают достаточно кислорода, потому что его количество, необходимое тканям, не соответствует количеству доступного переносчика (эритроцитов), это приводит к переходу клеток на бескислородное окисление, повышается уровень лактата, происходит метаболический ацидоз. Он, в свою очередь, приводит к ухудшению свертываемости крови, за которым следует угнетение обмена веществ и гипотермия, еще более острое падение уровня кальция (который также является фактором свертываемости), что снова приводит к кровопотере.
Данный процесс описывается как «Ромб смерти» (Lethal Dimond), в нем выделяется четыре основных патогенетических звена. Ранее гипокальцемия не выделялась в отдельное звено и процесс именовался «Треугольником смерти» или «Летальной триадой» (Lethal Triad). При этом применение кристаллоидов (особенно несбалансированных) не может решить указанные проблемы, а некоторые может усугубить.
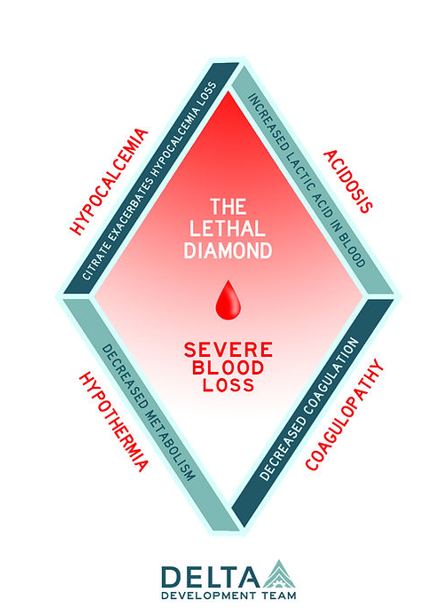
Физраствор усугубляет ацидоз и коагулопатию
Многочисленные исследования показали влияние физраствора даже на здоровых добровольцев, выявлены повышение уровня хлорида и снижение уровня бикарбонатов, снижение рН, тем самым наглядно продемонстрирован ацидотический эффект на здоровое не травмированное тело.
Поскольку этот эффект наблюдается у здоровых людей, необходимость применения физраствора у пострадавших с травмой, итак подверженных метаболическому ацидозу и коагулопатии вызывает сомнение. Исследования моделей животных продемонстрировали значительный гиперхлоремический ацидоз при введении физраствора, подтверждают это и реальные данные о повышении смертности у пациентов с травмами при использовании физраствора во время реанимации.
Как метаболический ацидоз, усугубленный применяем физраствора, влияет на «Ромб смерти»?
Было показано, что индуцированный ацидоз напрямую снижает сократительную способность сердца, а также снижает эффективность катехоламинов в кровеносном русле (например, адреналин). Кроме того, ацидотические состояния значительно снижают концентрацию фибриногена и нарушают выработку тромбина, что приводит к негативному влиянию на системы, необходимые для остановки кровотечения. Таким образом, основываясь только на ацидотическом характере физраствора, от его использования можно отказаться.
При тяжелой травме эффективная коагуляция жизненно важна для предотвращения дальнейшей кровпотери.
При травме коагулопатия может быть двух направлений – острая травматическая и ятрогенная (спровоцированная вмешательством медика). Непосредственно вторую и вызывает спасатель, когда применяет физраствор, нарушая функционирование тромбина и фибрина, которые необходимы для образования кровяного сгустка.
Физраствор не содержит факторов свертывания и не поддерживает свертывание крови, фактически, поскольку он еще больше разбавляет факторы коагуляции и повышает кислотность среды, может значительно ухудшить способность организма к остановке кровотечения и достижению гемостаза.
Гемодилюция (разбавление крови) и сосудистые изменения
Исследования доказали, что введение любых кристаллоидных растворов может оказывать сосудорасширяющий (вазодилатирующий) эффект, что наиболее выражено у физраствора. Также доказано, что что только 20% вводимого объема физраствора остается в сосудистом русле, что делает болюсное введение (быстрое в/в введение препарата в большом объеме и/или высокой концентрации) бесполезным.
Итак, физраствор расширяет сосуды, что оказывает дополнительную нагрузку на сердечно-сосудистую систему в дополнение к нагрузке, вызванной метаболическим ацидозом и кровопотерей.
Кроме того, физраствор оказывает значительное влияние на другой орган: почки — важный центр метаболизма, абсорбции (всасывания), реабсорбции и экскреции (выведения) ионов (в том числе хлорида и натрия) и регуляции кислотно-щелочного баланса.
На фоне сосудорасширяющих эффектов физраствора почечный кровоток и тканевое кровоснабжение (перфузия) значительно снижаются, тем самым, не допуская регуляции ионного и кислотно-щелочного дисбаланса.
Еще раз: при введении физраствора в одном месте сосуды расширяются, в почках кровоток снижается, они перестают в должной мере поддерживать гомеостаз (равновесие всех жидкостей, ионов и метаболитов организма), на фоне кровопотери и нахождения организма в шоковом состоянии это приводит к тому, что введение кристаллоида в попытке стабилизировать давление может убить пострадавшего.
Выводы
Каждый из пунктов, которые обозначены выше, можно разделить на несколько, развернуть каждый из них и обсудить отдельно, что мы обязательно сделаем в следующих статьях, посвященных патогенезу шока и другим состояниям.
Отдельно обозначим характеристики и побочные эффекты физраствора:
– История его создания не прозрачна, он никогда не был «физиологичным»;
– Изначально не предназначался для использования при травмах;
– Физраствор – не кровь и очень плохо ее имитирует;
– Применение может нанести существенный вред и усугубить текущее состояние пострадавшего.
Наконец, отметим, что допустимо применение физраствора при других состояниях, связанных с потерей жидкости, но не при кровотечениях.
Существуют рекомендации, допускающие коррекцию относительной гиповолемии (недостатка объема циркулирующей крови) с помощью кристаллоидов при, например, продолжительной диарее (холера, дизентерия) или при ожогах.
Источники:
Josh Farkas. Get SMART: Nine reasons to quit using normal saline for resuscitation.
Three Reasons Not to Use Normal Saline or Crystalloids in Trauma. Andrew D. Fisher, Brandon M. Carius, 03.14.2018
2022 Mar 12. The History of Intravenous and Oral Rehydration and Maintenance Therapy of Cholera and Non-Cholera Dehydrating Diarrheas: A Deconstruction of Translational Medicine: From Bench to Bedside? David R. Nalin
05 April 2013. The First Use of Intravenous Saline for the Treatment of Disease: Letter from Thomas Latta submitted to the Central Board of Health, London and published in The Lancet, 1832. Preface by Jane Ferrie.
2008. The history of 0.9% saline. Simon P Allison, Dileep N Lobo
Chen L. The myth of 0.9% saline: Neither normal nor physiological. Crit Care Nurs Q. 2015;38(4):385—389.
O’Shaughnessy WB. Experiments on the blood in cholera. Lancet. 1831;17(35):490.
Lewins R. Injection of saline solutions in extraordinary quantities into the veins of malignant cholera. Lancet. 1832;18(456):243—244.
Hamburger HJ. A Discourse on permeability in physiology and pathology. Lancet. 1921;198(5125):1039—1045.
Churton DR. Leeds general infirmary: A case of scirrhus of the pylorus, with excessive vomiting; repeated intravenous injections of saline solution; remarks. Lancet. 1888;132(3396):620—621.